2023-10-26 11:03:54
不同类型金属有机骨架材料合成及载雷公藤红素工艺研究
雷公藤红素(celastrol,Cel)是从雷公藤根皮中分离得到的五环三萜类活性化合物,分子式为C 29H 38O 4。现代药理研究表明,雷公藤红素具有抗肿瘤、抗炎、抗肥胖、免疫抑制及镇痛等药理活性,Cell杂志将其列为最有可能发展为药物的五种天然产物之一[1-5]。近年来,其抗肿瘤研究逐渐增多,雷公藤红素对前列腺癌、肺癌、肝癌、白血病、结肠癌、卵巢癌、乳腺癌等肿瘤细胞具有明显的抑制作用[6-10]。然而,在生物药剂学分类系统(BCS)中,雷公藤红素属于BCS II类,其难溶于水,溶出慢,生物利用度低及大剂量下的肝肾毒性限制了其临床应用[11-12]。近年来纳米载体的发展为雷公藤红素的应用提供了新方向。An等[13]制备了聚合物胶束用于雷公藤红素的递送以改善其水溶性,延长半衰期。Jin等[14]使用介孔二氧化硅装载雷公藤红素,制得的纳米粒子可改善其溶解度和生物利用度。
传统无机多孔材料如介孔二氧化硅、石墨烯等,其作为药物载体载药量高,但是存在体内不易降解等不足;有机材料如纳米脂质体、胶束等可体内降解完全,但载药量相对较低。金属有机骨架材料(metal organic frameworks,MOFs)作为一类新兴的多孔材料,近年来在药物载体领域发展迅速。其是由金属离子或金属团簇与有机配体通过配位键,辅助以范德华力或氢键等相互作用,自组装形成的一类具有无限周期性网络结构的聚合物材料。MOFs具有种类多样性、孔径可调、可表面修饰及大比表面积等优势,可兼顾载药量与体内可降解性。目前,研究较多的主要有IRMOFs系列(isoreticular metal organic frameworks)、MILs系列(material institute lavoisier frameworks)、ZIFs系列(zeoliticim idazolate frameworks)、PCNs系列(porous coordination networks)、UIOs系列(university of oslo)以及CPLs系列(coordinational pillared layers),见表1。
本研究选择在药物载体领域最常用的3种MOFs:UIO-66、ZIF-8与MIL-101(Fe),以粒径大小为指标,对其制备工艺进行正交优选,并对制备MOFs的晶体性质、形貌特征进行表征。筛选适宜MOFs,考察其对雷公藤红素的载药性能,同时对载药材料对HepG2细胞的细胞药效进行了初步评价,为后续体内外研究提供基础。
1仪器与材料
Mettler Toledo XP105型电子分析天平,梅特勒-托利多集团;DHG-9030A型鼓风干燥箱,上海一恒科学仪器有限公司;聚四氟乙烯内衬不锈钢反应釜,上海予申仪器有限公司;真空干燥箱,上海一恒科学仪器有限公司;S3400扫描电子显微镜(SEM),日本日立公司;Zetasizer Nano S90马尔文纳米粒径仪,英国马尔文公司;Rigaku UItima IVX射线衍射仪(XRD),日本理学公司;LC-20AT型高效液相色谱仪,日本岛津公司;F7000型荧光光谱仪,日本日立公司。
HepG2细胞购买于广州吉妮欧生物科技有限公司;四氯化锆,批号C11495248,质量分数>98%,上海麦克林生化科 技有限公司;对苯二甲酸、三氯化铁,分析纯,天津福晨化学试剂有限公司;N, N - 二甲基甲酰胺(DMF),冰醋酸、盐酸、磷酸、六水和硝酸锌,分析纯,国药集团化学试剂有限公司;苯甲酸、二甲基咪唑,分析纯,天津光复科技发展有限公司;雷公藤红素,批号YRL0094201022,质量分数>98%,宝鸡翊瑞生物科技有限公司;DMEM高糖培养基、胎牛血清、青链霉素混合液、CCK8染色液,北京索莱宝科技有限公司;甲醇,色谱纯,赛默飞世尔科技有限公司;水为娃哈哈纯净水。
2方法与结果
2.1UIO-66制备工艺考察
2.1.1溶剂热法合成UIO-66 分别精密称定适量四氯化锆和对苯二甲酸,加入一定体积DMF充分溶解,加适量调节剂。将反应液转移至50 mL聚四氟乙烯内衬的不锈钢反应釜内,在干燥箱内升温至120 ℃,恒温反应,反应结束后取出产物。12 000 r/min离心(离心半径75 mm)5 min,收集,沉淀分别依次用DMF和甲醇洗涤3次,置于真空干燥箱内室温干燥24 h。
2.1.2调节剂种类单因素考察比较不同种类调节剂乙酸、盐酸与苯甲酸对UIO-66的影响,其余制备条件一致。使用纳米粒径仪分别测定其粒径分布和多分散指数(polydispersity index,PDI)。表2结果表明,使用苯甲酸作为调节剂时,粒径较小且PDI值小于0.3,表明粒子分布较均匀。
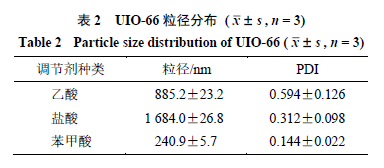
2.1.3UIO-66 制备正交试验考察以粒径大小为指标,苯甲酸作为调节剂,采用3因素3水平正交实验设计,考察投料比(A)、溶剂量(B)、反应时间(C)对UIO-66粒径大小的影响。正交试验的因素水平、实验设计与结果以及直观分析见表3,方差分析见表4。
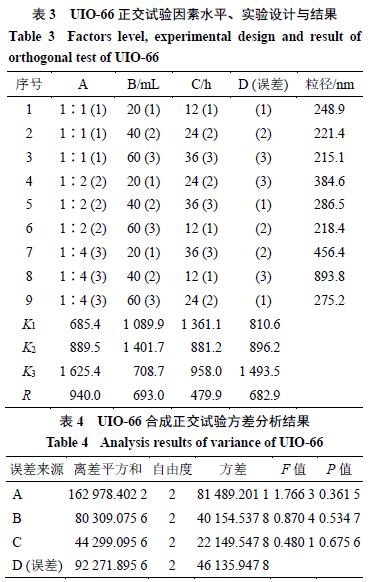
方差分析结果表明,3因素各水平无显著性差异。由直观分析可知,各因素对实验结果的影响依次为A>B>C,表明投料比对粒径影响较大。因素水平分析(K值分析)A为K3>K2>K1,A 1 粒径最小,即投料比四氯化锆-对苯二甲酸为1∶1;B为K2>K1>K3,B 3 粒径最小,即溶剂量60 mL;C为K1>K3>K2,C 2 粒径最小,即反应时间24 h。故UIO-66合成素最佳条件为A 1 B 3 C 2 ,即投料比1∶1,溶剂60 mL,反应24 h,此时制得UIO-66粒径最小。对A 1 B 3 C 2 进行3批验证,结果见表5。

3批验证结果表明,UIO-66合成工艺稳定可行,平均粒径为172.3 nm,分散性良好。
2.2 ZIF-8 制备工艺考察
2.2.1室温搅拌法合成ZIF-8 精密称取2-甲基咪唑溶解于一定体积溶剂中,精密称取六水硝酸锌溶解于少量溶剂中。在室温搅拌下,将六水硝酸锌溶液逐滴滴加至2-甲基咪唑溶液中,密闭搅拌一段时间,ZIF-8纳米粒自发形成,得到白色混悬液。12 000 r/min离心(离心半径75 mm)5 min,得到白色沉淀,甲醇洗涤3次,室温下真空干燥。
2.2.2溶剂种类比较ZIF-8 合成常用溶剂有水、甲醇、氨水及DMF,其余条件保持一致,比较分别使用4种溶剂制备ZIF-8粒径差异,结果见表6。水为溶剂合成ZIF-8粒径在200 nm左右,甲醇为溶剂合成ZIF-8粒径在600 nm左右,PDI均较低,分散均匀。12%氨水为溶剂合成ZIF-8粒径在250 nm左右,PDI较高,而DMF为溶剂室温下无明显产物出现,推测可能因为DMF常用于溶剂热法合成ZIF-8,室温合成法不适用。经比较,初步选择水作为合成溶剂制备ZIF-8。
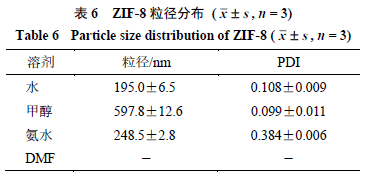
2.2.3 ZIF-8合成正交试验考察以粒径大小为指标,水为合成溶剂,采用3因素3水平正交试验设计,考察投料比(A)、溶剂量(B)、反应时间(C)对ZIF-8粒径大小的影响。因素水平表、实验设计与结果以及直观分析见表7,方差分析见表8。
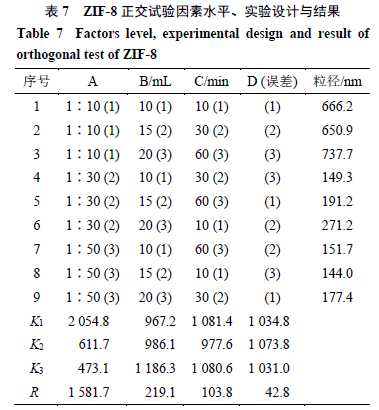
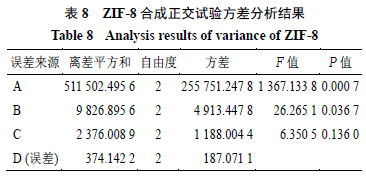
方差分析结果表明,A因素投料比与B因素溶剂量有显著性差异,C因素反应时间无统计学差异;由直观分析表可知,ZIF-8合成最优工艺为A 3 B 1 C 2 ,即投料比1∶50,溶剂10 mL,反应30 min。对A 3 B 1 C 2 进行3批验证,结果见表9。
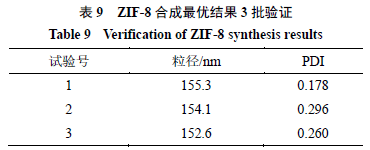
3批验证结果表明,ZIF-8合成工艺稳定可行,粒径均在154 nm左右,分散性良好。
2.3 MIL-101 (Fe)合成正交试验考察
2.3.1溶剂热法合成MIL-101(Fe)分别精密称适量三氯化铁和对苯二甲酸,加入一定体积DMF充分溶解,加适量调节剂。将反应液转移至50 mL聚四氟乙烯内衬的不锈钢反应釜内,在干燥箱内升温至110 ℃,恒温反应,反应结束后取出产物。12 000 r/min离心(离心半径75 mm)5 min收集,沉淀分别依次用DMF和甲醇洗涤3次,置于真空干燥箱内室温干燥24 h。
2.3.2MIL-101 (Fe)合成正交试验以粒径大小为指标,采用3因素3水平正交试验设计,考察投料比(A)、溶剂量(B)、反应时间(C)对MIL-101(Fe)粒径大小的影响。因素水平表、实验设计与结果以及直观分析见表10,方差分析见表11。
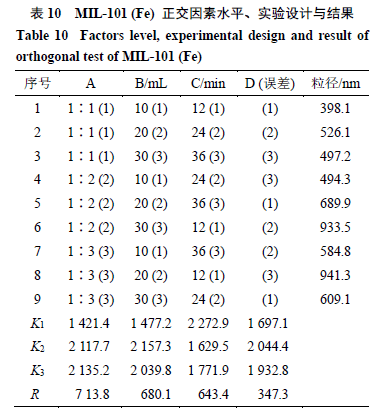
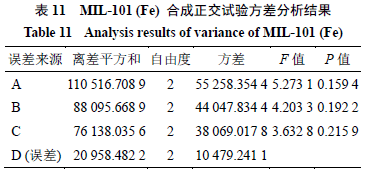
方差分析结果表明, 3因素均无显著性差异;由直观分析表可知,MIL-101(Fe)合成最优工艺为A 1 B 1 C 2 ,即投料比1∶1,溶剂10 mL,反应24 h。对A 1 B 1 C 2 进行3批验证,结果见表12。
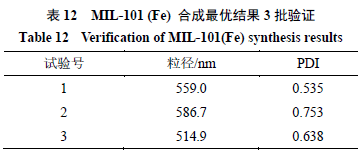
3 批MIL-101(Fe)粒径均在550 nm左右,工艺较稳定。但粒子PDI均较大,分布不均匀。
2.43种MOFs粒子的表征
使用SEM和XRD分别对上述合成的3种MOFs粒子的形貌大小和晶体特征进行表征。
2.4.1SEM 取粉末样品各微量,甲醇超声分散后,滴1滴于空白玻片表面,室温挥干溶剂,在样品表面喷金2.5 min后,进行SEM观察,记录SEM图谱,观察晶体形貌大小。3种材料的SEM形貌如图1所示。UIO-66粒子呈类球形多面体形状,粒子大小均匀,形状规则;ZIF-8呈六面体形状,分散均匀,粒径较小;MIL-101(Fe)呈八面体形,形状规则,但粒子大小有差异,均匀性较差。

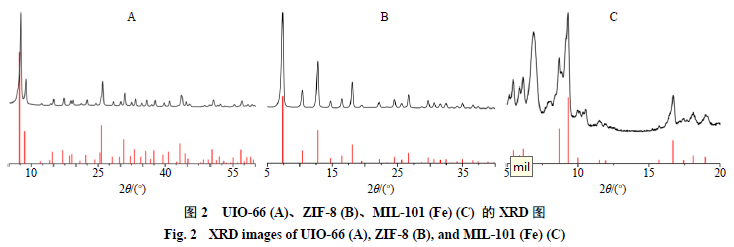
2.4.2XRD 取样品粉末各10 mg左右,在Cu-Kα(λ=1.541 nm),高压40 kV,管流40 mA,扫描速度2°/min的条件下进行X射线衍射,得到衍射图谱(图2),测定样品的结晶度和纯度。UIO-66在2 θ 7.54 °、8.70°、25.90°、30.90°等处的衍射峰与文献报道一致[20],且无其他材料衍射峰出现。ZIF-8衍射峰在2 θ 7.50 °、10.54°、12.90°、16.62°及18.20°,均符合文献已报道的ZIF-8衍射峰[21]。MIL-101(Fe)在2 θ 5.44 °、8.70°、9.30°、10.52°及16.68°处均出现明显的吸收峰,与已报道的MIL-101型的标准XRD特征峰一致[22]。
综合上述合成及表征结果,ZIF-8制备简便,粒径小,分布均匀,工艺稳定,较符合药物载体要求选择ZIF-8进行后续载药实验。
2.5 ZIF-8 装载雷公藤红素制备纳米粒(ZIF-8@ Cel)的性能研究
2.5.1ZIF-8 装载雷公藤红素工艺采用吸附法进行载药。将适量ZIF-8粉末置于雷公藤红素甲醇溶液中,室温密闭搅拌一定时间,12 000 r/min离心(离心半径75 mm)5 min,甲醇多次洗涤,室温下真空干燥,即得ZIF-8@Cel载药纳米粒。
2.5.2载药量测定
(1)雷公藤红素色谱条件:色谱柱为Agilent Zorbax Eclipse plus C 18 柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.1%磷酸水水溶液(80∶20),等度洗脱;体积流量1.0 mL/min;柱温35 ℃;检测波长244 nm;进样量10 μL。
(2)对照品溶液的制备:精密称取雷公藤红素5 mg于10 mL量瓶中,加甲醇溶解并稀释至刻度,作为储备液。精确量取储备液2 mL于5 mL量瓶中,加甲醇稀释至刻度,即得含雷公藤红素0.2 mg/mL的对照品溶液。
(3)供试品溶液的制备:取ZIF-8@Cel约5 mg,精密称定,加1 mL冰醋酸,加适量甲醇超声处理(功率150 W、频率40 kHz)20 min,定容至10 mL量瓶中,摇匀,即得。
(4)阴性供试品溶液的制备:取空白材料约5 mg,精密称定,按照“2.5.2(2)”项方法制成阴性供试品溶液。
(5)专属性考察:分别吸取对照品溶液、供试品溶液和阴性供试品溶液各1 mL,经微孔滤膜滤过后,按照“2.5.2(1)”项下色谱条件,进高效液相检测,色谱图见图3。
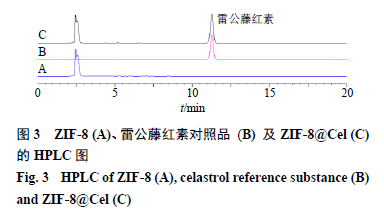
(6)线性关系考察:精密称取雷公藤红素对照品5.0 mg置于10 mL量瓶中,甲醇定容至刻度,配制成质量浓度为0.5 mg/mL的对照品母液。精密吸取母液适量,依次用甲醇稀释,得到质量浓度分别为0.2、0.1、0.05、0.02、0.01、0.005 mg/mL系列对照品溶液。按“2.5.2(1)”项下方法检测,以峰面积为纵坐标(Y),质量浓度为横坐标(X),绘制标准曲线并进行线性回归,得雷公藤红素的回归方程为Y=12 125 696.90 X +14 234.01,R2=1.000 0, 表明雷公藤红素在0.005~0.5 mg/mL线性关系良好。
(7)检测限与定量限:精确吸取“2.5.2(2)”项中对照品溶液,甲醇稀释,按照“2.5.2(1)”项色谱条件进行测定。样品峰高为仪器噪声高度3倍时的样品质量浓度即为样品的检出限,样品峰高为仪器噪声高度10倍时的样品质量浓度即为样品的定量限。结果显示,雷公藤红素的检测限为0.06 μg/mL,定量限为0.20 μg/mL。
(8)精密度试验:精密吸取质量浓度为0.2 mg/mL的雷公藤红素对照品溶液1 mL,按照“2.5.2(1)”项下色谱条件每天连续进样6次,连续进样3 d,记录峰面积,计算RSD值。结果日内精密度RSD为1.62%,日间精密度RSD为0.32%,表明其精密度良好。
(9)稳定性试验:精密移取ZIF-8@Cel供试品溶液1 mL,按照“2.5.2(1)”项下色谱条件,分别在0、2、4、8、12、24 h进样,记录峰面积,计算RSD值,测得峰面积的RSD值为0.37%,表明供试品溶液在24 h内稳定。
(10)重复性试验:重复制备6份ZIF-8@Cel供试品溶液,分别精密吸取上述供试品溶液各1 mL,按照“2.5.2(1)”项下色谱条件进样测定。结果ZIF-8@Cel样品中雷公藤红素的平均载药量为23.36%,其RSD值为1.15%,表明测定方法的重复性良好。
(11)加样回收率试验:精密称定ZIF-8@Cel样品2.5 mg,加入0.5 mg/mL对照品溶液1 mL,按照“2.5.2(3)”项下方法制备加样回收供试品溶液6份,测得加样回收率为97.77%,RSD小于5%,表明该方法回收率符合要求。
2.5.3ZIF-8@CEL 载药工艺单因素考察
(1)ZIF-8与雷公藤红素质量比考察:根据文献调研及预实验结果,设置ZIF-8与雷公藤红素质量比分别为1∶2、1∶1、2∶1、3∶1,药液质量浓度5 mg/mL,载药时间24 h,比较载药粒子粒径大小及载药量。结果(表13)表明,随着ZIF-8比例的增大,粒径呈减小趋势,变化幅度逐渐减小,比例为2∶1与3∶1粒径接近;载药量随着ZIF-8比例的增大而减小。综合粒径与载药量结果,选择ZIF-8与CEL比例2∶1进行后续实验。
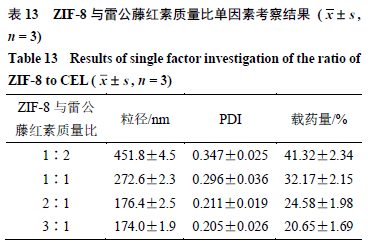
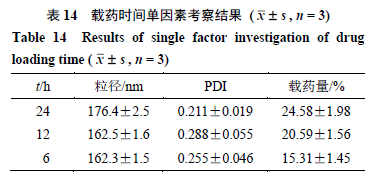
(2)载药时间考察:载药时间的长短也对载药行为影响较大。暂定ZIF-8与CEL比例2∶1,药液质量浓度5 mg/mL,设置载药时间24、12、6 h进行考察。结果(表14)表明,时间越短粒子粒径越小,载药量越低,最终确定载药时间24 h。
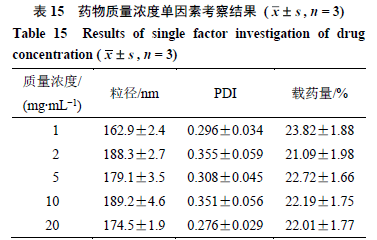
(3)药液质量浓度考察:固定ZIF-8与CEL比例2∶1,载药时间24 h,比较药液质量浓度1、2、5、10、20 mg/mL的影响。结果(表15)表明,药物质量浓度为1 mg/mL时,粒径相对较小,同时载药量较高。
综合上述单因素结果,确定最佳载药工艺为ZIF-8与CEL质量比2∶1,载药时间24 h,药物质量浓度为1 mg/mL。进行3批最佳工艺验证,结果ZIF-8@CEL的平均粒径为(164.9±8.0)nm,PDI为0.297±0.029,载药量为(23.47±0.26)%,工艺稳定可行。
2.6细胞水平药效评价
HepG2细胞在含有10%胎牛血清和抗生素(100 µg/mL青霉素和100 µg/mL链霉素)的DMEM高糖培养基中,在37 ℃、5% CO 2 下培养2~3 d。
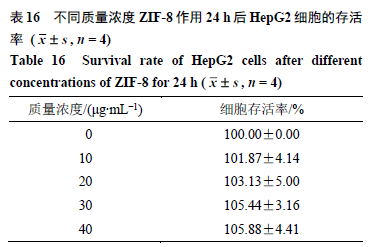
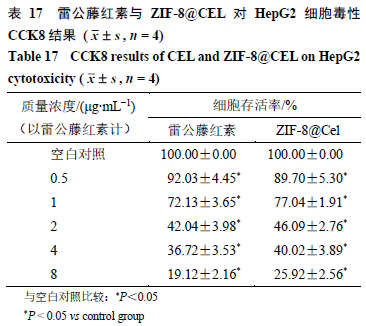
在比较游离CEL和ZIF-8@CEL的细胞毒性作用之前,采用CCK-8法检测空白ZIF-8对HepG2细胞的体外细胞毒性。当细胞覆盖培养瓶底部的80%以上面积时,用胰蛋白酶消化收集细胞,并在新鲜培养基中重悬。细胞接种于96孔板,接种密度为100 μL/孔,接种数量为6000个/孔,培养过夜。然后用不同质量浓度的ZIF-8处理细胞24 h,弃上清液,每孔加入含10% CCK-8的100 μL培养基溶液,37 ℃避光孵育3 h。用酶标仪测定了在450 nm波长处的吸光度(A)值。根据表16,不同质量浓度的ZIF-8(0、10、20、30、40 μg/mL)孵育24 h后,细胞存活率无显著降低,说明ZIF-8在实验剂量下是无毒的。接着,CCK-8法比较了游离雷公藤红素和ZIF- 8@CEL对HepG2细胞的毒性。结果(表17)显示随着质量浓度升高,细胞存活率逐渐降低,具有明显质量浓度相关性。雷公藤红素的半数致死浓度(half-inhibitory concentration,IC 50 )值为3.821 μg/mL,ZIF-8@CEL的IC 50 值为3.289 μg/mL(以雷公藤红素计)。含相同质量浓度雷公藤红素条件下,ZIF-8@CEL对HepG2细胞抑制效果更强,IC 50 值更小。
3讨论
MOFs结合了有机材料的可降解性及无机材料的高载药量的优势。其是由金属配位键、范德华力等作用力结合,其相对较弱的结合力会在体内被逐渐解离,变为小分子有机物及金属离子,小分子可直接被代谢,金属离子为体内存在的锌、铁等离子,可被吸收代谢,具有良好的安全性[23]。Baati等[24]制备了MIL88B、MIL88A及MIL100等多种铁基MOFs,并静脉注射到大鼠体内,发现其在体内会被肝脏和脾脏分解成铁离子和有机配体,并通过尿液和粪便排除,基本不存在代谢毒性。
本实验选择的3类MOFs分别属于UIOs系列、ZIFs系列与MILs系列。文献研究表明,这3类MOFs在生物医药领域的应用较多。UIO-66、ZIF-8与MIL-101(Fe)分别为3类MOFs中的代表,其金属中心依次为四价锆、二价锌及三价铁,包括了不同金属类型及价位,且3类材料具有不同的晶体结构,具有良好的代表性。目前,这3种MOFs作为药物载体的研究受到较多关注[25-26]。Haddad等[27]使用UIO-66负载抗肿瘤药物二氯乙酸,同时修饰了定位于线粒体的三苯基膦,具有良好的抗肿瘤效果和靶向性。Zhang等[28]使用ZIF-8负载抗肿瘤前药,进一步使用透明质酸功能化修饰,制备的纳米粒子具有良好的抗肿瘤效果。Cai等[29]将叶酸和5-羧酸荧光素用于修饰MIL-101(Fe)以构建功能化纳米平台,同时递送抗肿瘤药物雷公藤甲素,具有优异的荧光成像和协同靶向抗癌活性。本实验通过单因素考察结合正交试验分别对3类MOFs的合成工艺进行了优化,得到最佳制备工艺。经比较,ZIF-8粒径在154 nm左右,形状规则,晶型良好,分布均匀,适宜作为药物载体用于后续实验。
对于CEL的包载,常用方法有“一步法”与吸附法。“一步法”为药物与合成原料同时加入,在材料合成的同时,将药物分子包裹在材料孔隙内;吸附法为先合成空白材料,再将材料置于一定质量浓度药液中密闭搅拌一定时间,依靠材料吸附性进行药物装载。前期预试验发现,“一步法”制备的载药粒子载药量均较低,增加药物浓度以提高载药量的同时,粒径也急剧增大,载药量5%左右时粒径接近900 nm。经分析可能是由于雷公藤红素中含有羧基基团,其在二甲基咪唑形成的碱性溶液里与金属离子配位结合产生络合物,导致形成的ZIF-8金属中心数量少,粒子粒径大,同时载药量较低。因此最终采用吸附法进行载药,通过单因素试验,考察影响吸附法载药的3个因素载体药物比、载药时间与药物浓度,最终确定载药工艺为ZIF-8与雷公藤红素比例2∶1,载药时间24 h,药物质量浓度为1 mg/mL,得到ZIF-8@CEL粒径为165 nm左右,分散均匀,载药量约23%,工艺稳定可行。
最后,CCK-8细胞毒性试验评价了ZIF-8、CEL及ZIF-8@CEL对HepG2细胞的抑制作用,结果表明ZIF-8在实验剂量下安全性良好,ZIF-8@CEL相较于雷公藤红素抑制效果更强,IC 50 值更小。后续细胞毒性机制及体内抗肿瘤试验将进一步验证纳米载体的优势。
推荐新闻
-
发布时间 | 2024-08-06 13:47:51
德尔塔生物提供质粒及细胞系构建定制服务
-
发布时间 | 2024-07-03 10:24:17
水凝胶涂覆的MOF纳米粒子用作刺激响应的可控药物释放
-
发布时间 | 2024-07-03 10:20:24
Fe@γ-Fe2O3@H-TiO2的多面应用——从光催化到多模态成像介导的癌症光热治疗
-
发布时间 | 2024-06-06 17:40:56
生物功能电纺纳米材料——从拓扑结构设计到生物应用
-
发布时间 | 2024-05-22 15:01:40
GelMA气凝胶作为新型的电子皮肤材料
-
发布时间 | 2024-05-22 14:59:05
PDMS改性硅气凝胶PDMS修饰的二氧化硅气凝胶膜层
-
发布时间 | 2023-11-29 14:56:26
构建多功能化的四氧化三铁杂化纳米平台用于癌症的诊断和治疗
-
发布时间 | 2023-11-07 11:36:34
荧光标记方法有这4种,小伙伴们知道吗?
-
发布时间 | 2023-10-26 11:03:54
不同类型金属有机骨架材料合成及载雷公藤红素工艺研究
-
发布时间 | 2023-10-26 10:59:50
一种开创性的微孔有机聚合物合成模板
-
发布时间 | 2023-10-26 10:58:09
超快速半干态合成高耐久性ZIF-8膜用于丙烯/丙烷分离
-
发布时间 | 2023-10-26 10:43:37
关于PEG120-PLGA-PEG-FA文献阅读
-
发布时间 | 2023-10-26 10:41:54
ZIF-8制备原位碳掺杂氧化锌及其光催化性能研究
-
发布时间 | 2023-10-26 10:40:20
ZIF-8修饰整体柱的制备及性能研究
-
发布时间 | 2023-10-26 10:39:01
反沙漠甲虫性能的ZIF-8/PAN功能膜用于水包油乳液的高效和快速分离

